






2025-10-24 05:28:34
當(dāng)實(shí)驗(yàn)室更換內(nèi)毒素檢測(cè)方法或更換試劑供應(yīng)商時(shí),需進(jìn)行方法比對(duì)與橋接驗(yàn)證。比對(duì)實(shí)驗(yàn)需選取至少 3批代表性樣品,分別用新舊方法檢測(cè),計(jì)算結(jié)果相關(guān)性(如相關(guān)系數(shù) R?≥0.95)和偏差(≤20%)。橋接驗(yàn)證還需評(píng)估新方法的特異性、靈敏度是否與舊方法一致,如確認(rèn)對(duì)高風(fēng)險(xiǎn)樣品(如含 β- 葡聚糖的樣品)的抗干擾能力相當(dāng)。若方法變更涉及法規(guī)申報(bào)產(chǎn)品,需將驗(yàn)證數(shù)據(jù)納入申報(bào)資料,證明變更后方法仍能有效控制內(nèi)毒素風(fēng)險(xiǎn),符合 FDA、NMPA 等監(jiān)管機(jī)構(gòu)對(duì)方法變更的合規(guī)性要求。 內(nèi)毒素檢測(cè)假陰性多因樣品抑制,梯度稀釋結(jié)合加標(biāo)試驗(yàn)可定位偏差原因。北京細(xì)菌內(nèi)毒素檢測(cè)常見(jiàn)問(wèn)題分析
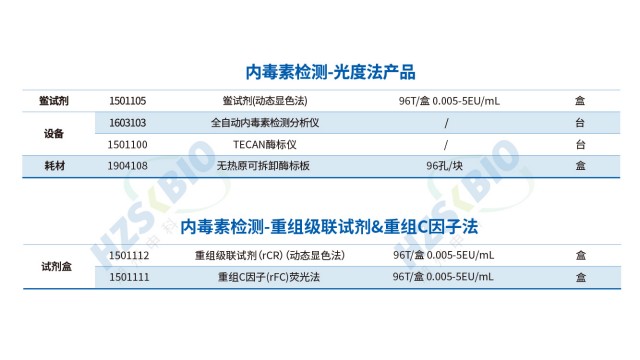
鱟試驗(yàn)法(LAL 法)是細(xì)菌內(nèi)毒素檢測(cè)的經(jīng)典方法,依據(jù)反應(yīng)監(jiān)測(cè)方式可分為三類:凝膠法、濁度法和顯色法。凝膠法通過(guò)觀察是否形成凝膠判斷內(nèi)毒素是否超標(biāo),其優(yōu)勢(shì)是操作簡(jiǎn)便、成本較低,適用于定性或半定量檢測(cè),如**器械初篩;濁度法通過(guò)監(jiān)測(cè)反應(yīng)體系濁度變化速率定量?jī)?nèi)毒素,靈敏度高(可達(dá) 0.005 EU/mL),適用于生物制品原液等高精度需求場(chǎng)景;顯色法基于顯色底物的吸光度變化定量,抗干擾能力較強(qiáng),適配復(fù)雜基質(zhì)樣品(如含蛋白質(zhì)的注射液)。三種方法均需嚴(yán)格控制反應(yīng)溫度(37℃±1℃)和時(shí)間,確保結(jié)果可靠性。 北京非動(dòng)物源內(nèi)毒素檢測(cè)方法驗(yàn)證細(xì)菌內(nèi)毒素試驗(yàn)(BET)是用鱟變形細(xì)胞裂解物(LAL)測(cè)內(nèi)毒素的體外方法,LAL 測(cè)試獲國(guó)際藥典推薦。
樣品中存在的非特異性鱟反應(yīng)啟動(dòng)物,會(huì)繞過(guò)內(nèi)毒素直接觸發(fā)鱟試劑反應(yīng),導(dǎo)致內(nèi)毒素檢測(cè)出現(xiàn)假陽(yáng)性,需針對(duì)性消除干擾。常見(jiàn)的非特異性啟動(dòng)物包括 1,3-β-D 葡聚糖和含絲氨酸蛋白酶的生物制品(如胰酶):1,3-β-D 葡聚糖會(huì)啟動(dòng)鱟試劑的 G 因子旁路,不依賴內(nèi)毒素即可引發(fā)凝膠形成或光度變化;胰酶等絲氨酸蛋白酶類物質(zhì),其作用機(jī)制與內(nèi)毒素觸發(fā)鱟試劑的過(guò)程相似,會(huì)模擬內(nèi)毒素信號(hào)導(dǎo)致誤判。針對(duì)這類干擾,若樣品含 1,3-β-D 葡聚糖,可使用試劑盒配套的抗增液,通過(guò)抑制 G 因子活性阻斷旁路啟動(dòng);若樣品為胰酶等生物制品,可通過(guò)加熱處理(如 80℃加熱 10 分鐘)滅活絲氨酸蛋白酶,避免其模擬內(nèi)毒素反應(yīng)。這些處理措施能有效排除非特異性信號(hào),確保內(nèi)毒素檢測(cè)只針對(duì)目標(biāo)內(nèi)毒素產(chǎn)生響應(yīng),提升結(jié)果準(zhǔn)確性。
低內(nèi)毒素回收(LER)與傳統(tǒng)鱟試劑干擾(抑制 / 增強(qiáng))在多維度存在差異,準(zhǔn)確區(qū)分對(duì)優(yōu)化內(nèi)毒素檢測(cè)至關(guān)重要。表現(xiàn)上,LER 是內(nèi)毒素回收率<50%,傳統(tǒng)干擾是反應(yīng)抑制或增強(qiáng);成因上,LER 由螯合劑 + 表面活性劑協(xié)同或蛋白質(zhì)電荷結(jié)合引發(fā),傳統(tǒng)干擾因 pH、β- 葡聚糖等導(dǎo)致;排除方式上,LER 時(shí)間依賴且無(wú)法稀釋解決,傳統(tǒng)干擾濃度依賴且可通過(guò)稀釋緩解;確認(rèn)方法上,LER 需通過(guò)保存時(shí)間研究(HTS),傳統(tǒng)干擾按藥典干擾實(shí)驗(yàn)評(píng)估。明確這些區(qū)別能幫助企業(yè)排查內(nèi)毒素檢測(cè)異常,避免誤將 LER 當(dāng)作普通干擾處理。 內(nèi)毒素檢測(cè)復(fù)孔 CV>15%,需校準(zhǔn)移液**,規(guī)范加樣,排查耗材污染。

湖州申科生物動(dòng)態(tài)顯色法鱟試劑用于定量測(cè)定人用和動(dòng)物用注射藥物、生物制品及**器械等樣本中的細(xì)菌內(nèi)毒素的含量。 細(xì)菌內(nèi)毒素能特異性地活化反應(yīng)主劑中的 C 因子,活化的 C 因子活化 B 因子,活化的 B 因子進(jìn)而活化凝固酶原,凝固酶水解反應(yīng)中的顯色底物,產(chǎn)生游離的pNA(對(duì)硝基苯胺)從而引起吸光度變化,根據(jù)動(dòng)態(tài)檢測(cè)溶液吸光度變化率對(duì)內(nèi)毒素進(jìn)行定量。本品能夠快速、高靈敏度地定量檢測(cè)樣品中的內(nèi)毒素水平,適用于各種實(shí)驗(yàn)室和工業(yè)生產(chǎn)場(chǎng)景,確保產(chǎn)品質(zhì)量和**性。 鱟試劑含多種酶和輔助因子,批次間活性差異可能導(dǎo)致內(nèi)毒素檢測(cè)結(jié)果變異性。江蘇血液制品內(nèi)毒素檢測(cè)操作步驟
重組鱟試劑無(wú)動(dòng)物源,支持 3R 原則,批次差異小,適配動(dòng)態(tài)顯色法酶標(biāo)儀。北京細(xì)菌內(nèi)毒素檢測(cè)常見(jiàn)問(wèn)題分析
內(nèi)毒素檢測(cè)中,樣品中的蛋白質(zhì)或酶的修飾作用易破壞鱟試劑的反應(yīng)體系,導(dǎo)致檢測(cè)結(jié)果失真。鱟試劑檢測(cè)內(nèi)毒素的本質(zhì)是一系列絲氨酸蛋白酶的酶促放大過(guò)程,若樣品中存在氧化劑、抗氧化劑、蛋白水解劑或?qū)R皇Щ顒瑫?huì)直接滅活反應(yīng)所需的酶;而乙醇、苯酚等物質(zhì)則會(huì)導(dǎo)致蛋白質(zhì)變性,同樣抑制反應(yīng)進(jìn)程。例如,某些生物制品中含有的蛋白水解酶,可能提前降解鱟試劑中的蛋白酶,使內(nèi)毒素?zé)o法被正常檢測(cè)。為消除這類干擾,需優(yōu)先限制樣品中抑制物的含量:可采用內(nèi)毒素檢查用水稀釋樣品,降低抑制物濃度;對(duì)耐熱的抑制物(如部分蛋白水解酶),可通過(guò)加熱滅活處理(如 56℃孵育 30 分鐘)破壞其活性;若樣品基質(zhì)復(fù)雜,還可使用超濾技術(shù)分離內(nèi)毒素與干擾蛋白質(zhì),避免修飾作用對(duì)酶促反應(yīng)的影響,保障內(nèi)毒素檢測(cè)結(jié)果的可靠性。 北京細(xì)菌內(nèi)毒素檢測(cè)常見(jiàn)問(wèn)題分析